产品搜索
联系我们
电话:4008750250
手机:18066071954
地址:南京市栖霞区纬地路9号
Email: zhangxiangwen@cobioer.com
技术文章 / article
【分享】NIST开发ERBB2- CNV标准品的一些思路
原载自:www.co-bioer.com[技术资料频道] 2022-02-22 浏览次数:2171
一般来说,拷贝数变异CNV(copy number variant)被定义为人类基因组中1kb或更大的DNA的片段的扩增或减少,CNV可以分为拷贝数扩增(copy number gain)和拷贝数缺失(copy number loss),在肿瘤细胞中,往往会出现原癌基因的扩增,抑癌基因的缺失,扩增和缺失一般会直接影响RNA和蛋白的表达,进而影响肿瘤的发生、发展,与肿瘤细胞的生长、药物敏感性、耐药性都密切相关。有数据表明,CNV在人类癌症基因组中普遍存在,比起单核苷酸多态性 (SNP) ,CNV影响更大的基因组片段。
基因CNV的检测有多种方法,包括Southern印迹杂交、荧光原位杂交(FISH)、聚合酶链反应(PCR)、比较基因组杂交(CGH)、全基因组单核苷酸多态性 (SNP) 阵列和NGS等,各有优点和缺点。
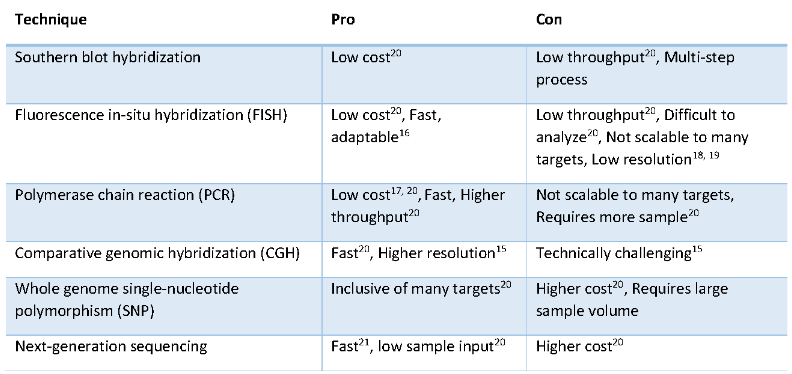
Fig 1. CNV检测技术比较
今天我们与大家分享一篇NIST(National Institute of Standards and Technology)的文章(点击即可查看文章内容),是他们开发2373标准物质的过程:针对HER2的gDNA标准品,主要是用于Q-PCR和dPCR的,当然也是适用于NGS,但是由于检测方法不同、分析方法不同,在定值上会与Q-PCR和dPCR不一致。
首先文章发现很多乳腺癌患者的样本存在大量的染色体结构异常,在开发Q-PCR和dPCR时,需要
选择内参基因,内参基因的选择要尽量避开染色体异常的区域。研究发现,这些乳腺癌样本在1q, 8q, 20q, 7, 11q, 13, 17q, 9q ,16p等区域经常发生基因的扩增,在8p, 11q14-qter, 18q, Xq等区域经常发生基因的缺失,同时内参基因的选择尽量不能在chr17(HER2基因的位置)上选择,因此文章最终选择了DCK基因、EIF5B基因、RPS27A基因和PMM1基因(其中PMM1仅用于Q-PCR实验)。

Table 1. HER2和内参基因的引物信息
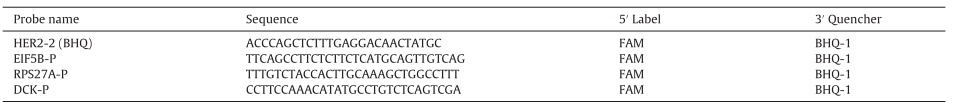
Table 2. HER2和内参基因的探针信息
作为一个标准品,需要尽量模拟临床样本,同时需要稳定的长久供应,因此文章选择了5个常见的乳腺癌细胞作为标准品的原材料,用于定标实验,分别为:SK-BR-3(components A), MDA-MB-231(components B), MDA-MB-361(components C), MDA-MB-453(components D)和 BT-474(components E),这些细胞经过培养,提取gDNA,STR鉴定,确保质量合格,备用于接下来的测试。
同时文章构建了一个HER2 cDNA的质粒,通过质粒的分子量,计算得到质量与拷贝数的对应关系,构建标准曲线,同时引入2372-A样本(全基因组DNA: gDNA),也构建质量与拷贝数的关系,通过Q-PCR检测,发现有很强的相关性,R2=0.9924,进而得到2372-A样本在二倍体时,对应HER2的拷贝数为2,进而可以用于components A-E的检测校准。
接下来对components A-E开展Q-PCR和dPCR的检测,Q-PCR采用4种内参基因,根据校正标曲计算得到A-E样本的copies/μL,dPCR采用3种内参基因,同时计算A-E样本的copies/μL和与内参基因的比值,在这里,文章中使用了2种dPCR的方法,分别为
droplet dPCR和chamber dPCR。
在计算上,首先通过质粒HER2 cDNA的Q-PCR数据,校正2372-A的gDNA样本,显示2372-A样本二倍体样本,HER2拷贝为2,再利用2372-A样本计算A-E样本的拷贝数值(copies/μL),dPCR则直接检测HER2和内参基因的拷贝数,进而计算比值。
最终文章显示首先2种dPCR采用3种内参基因,计算HER2与内参基因的比值,结果有很强的
一致性,5个样本出现不同程度的拷贝数扩增,有弱有强。
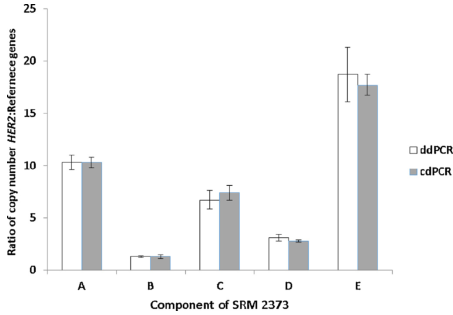
Fig 2. 针对A-E样本,2种dPCR的方法一致性较好。(数据为3种内参的平均值)
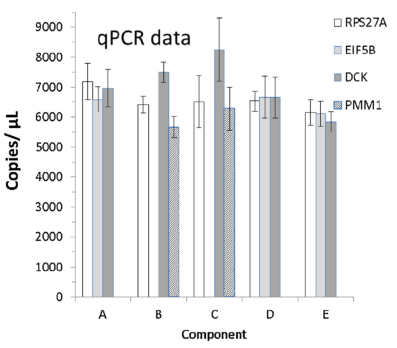
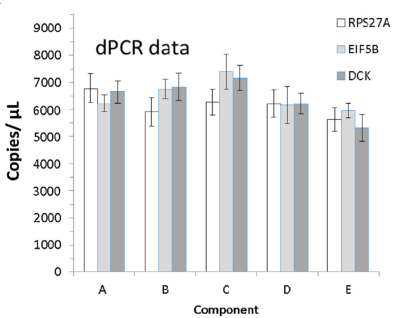
其次A-E样本在Q-PCR和dPCR上针对copies/μL也有很强的一致性,表明A-E标准品同时适用于Q-PCR和dPCR应用。
|
|
Fig 3. 左侧为A-E样本在Q-PCR检测中内参的拷贝数值,右侧为A-E样本在dPCR检测中内参的拷贝数值。 | |
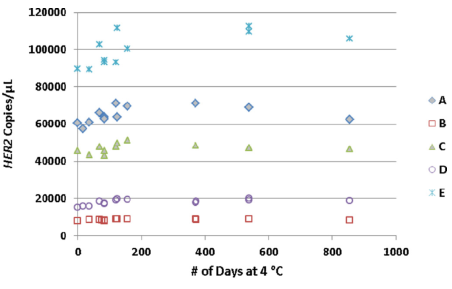
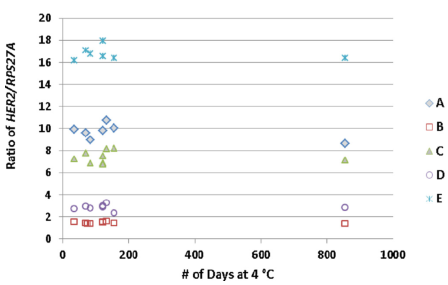
另外文章还检测了A-E样本的稳定性,在长达856天的测试中,不管是绝对的拷贝数,还是与内参的比值,都呈现良好的稳定性。
|
|
Fig 4. 不管是HER2的拷贝数值,还是与内参的比值,在856天的测试中,都较稳定。 | |
最后文章还测试了随机因素对A-E实验的重复性的影响,比如机器、操作者、日期等等,呈现良好的重复性。
综上可知,在开发CNV检测的分子诊断标准品时,我们需要注意:
● 可以设置绝对的拷贝数值(copies/μL)作为标准,可以使用dPCR和Q-PCR定标,其中Q-PCR需要使用校正标曲;
● 可以设置与内参基因的比值,作为标准,适合dPCR的方法(Q-PCR也可以,同样需要校正标曲),这时需要注意内参的选择原则,如果可以的话,尽量多选择几个内参基因;
● 标准品需要稳定供应,需要测试长久的稳定性,测试在不同的随机因素下的重复性;
但是我们发现还是有一些问题没有解决,比如:Q-PCR和dPCR都是很短序列的PCR反应,在整个HER2基因的什么
区段选择扩增?不同区段的扩增效率会直接影响拷贝数值(copies/μL),进而不同区段检测得到的拷贝数与内参基因的比值也会不一致,甚至是否会出现PCR反应正好设计在各个拷贝的差异处,就不仅仅是扩增效率的问题了。
另外在文章之外,我们可以
探讨下:这个标准品是否适用于NGS?我们知道NGS是比较各处的测序深度,进而判断区域的拷贝数,与Q-PCR和dPCR的检测方法差异很大,看起来NGS会检测到不一样的结果。