产品搜索
联系我们
电话:4008750250
手机:18066071954
地址:南京市栖霞区纬地路9号
Email: zhangxiangwen@cobioer.com
技术文章 / article
TSHR细胞模型简介
原载自:www.co-bioer.com[技术资料频道] 2026-01-16 浏览次数:390
背景
在过去十年中,甲状腺癌的发病率显著上升。 分化型甲状腺癌(DTC)占甲状腺癌患者的96%,治疗方法通常是手术治疗,随后进行甲状腺刺激激素(TSH)抑制治疗和放射性碘治疗。促甲状腺激素受体(TSHR)是位于甲状腺细胞表面的G蛋白偶联受体,通过结合促甲状腺激素(TSH)激活Gs信号通路,调控甲状腺素(T4)和三碘甲状腺原氨酸(T3)的合成与分泌。维持甲状腺细胞的正常生长和增殖,调节碘代谢,并介导甲状腺激素的合成和分泌。通过腺苷酸环化酶信号通路,TSHR参与能量代谢和生长等关键过程。TSHR在DTC中独特作用及其作为治疗靶点的潜力,使其成为深入研究的焦点。探索TSHR的生物功能及其在DTC中的机制对于开发新颖治疗策略至关重要。
TSHR的结构与功能
TSHR蛋白包括三个结构域:细胞外结构域、跨膜结构域和细胞内结构域。胞外结构域包含418个亲水氨基酸,包括一个富含亮氨酸的重复(LRR)结构域和一个铰链区,这些区域与垂体分泌的TSH密切结合。此外,TSHR细胞外结构域包含六个高度保守的糖基位点,这种糖基化对于维持受体稳定性和功能至关重要,促进TSHR定位到细胞膜,并通过延长受体停留时间增强TSH结合。TSH结合会在TSHR胞外结构域产生直立主动构象,进而触发跨膜结构域的构象变化,最终激活细胞内G蛋白信号通路。跨膜结构域由七个螺旋段组成,是TSHR中介导信号转导的主要结构元素。
TSHR通过其细胞内结构域与G蛋白结合,主要通过Gs蛋白启动信号转导。Gs通路的激活增加了环腺苷单磷酸(cAMP)的丰度,而cAMP激活蛋白激酶A(PKA)。PKA磷酸化下游分子,调控甲状腺过氧化物酶(TPO)和钠/碘共运蛋白(NIS),从而促进甲状腺激素的合成和分泌。除了Gs通路外,TSHR还通过Gq蛋白传递信号,Gq蛋白激活磷脂酶C(PLC),将PIP2水解为肌醇三磷酸(IP3)和二酰甘油(DAG)。DAG和PKA都能刺激蛋白激酶C(PKC)进而激活AKT通路,影响细胞存活、增殖、生长和糖原代谢。TSHR信号传递也与MAPK/ERK级联有功能关联。

靶向TSHR的药物研发进展
靶向治疗带来了癌症治疗的革命性变化。精确地将药物输送到特定组织,有效减少副作用,扩大治疗窗口,并提高药物疗效。复发或转移性甲状腺癌患者通常需要积极治疗,伴随多种不良反应。TSHR作为甲状腺功能的关键调节因子,现已成为治疗DTC的关键靶点。基于TSHR的治疗方法,包括小分子化药、细胞疗法(CAR-T)和纳米材料等,代表了治疗甲状腺癌的新途径,特别是针对那些对传统治疗(如放射性碘治疗)产生耐药性的患者。

目前靶向TSHR已上市的药物,主要是作为TSHR激动剂的激素类药物,广泛应用于分化型甲状腺癌的治疗,如由苏州智核生物医药科技有限公司研发的Recombinant human thyroid stimulating hormone(SmartNuclide)、由Sanofi研发的Thyrotropin Alfa以及由苏州泽璟生物制药股份有限公司研发的Recombinant human thyrotropin。
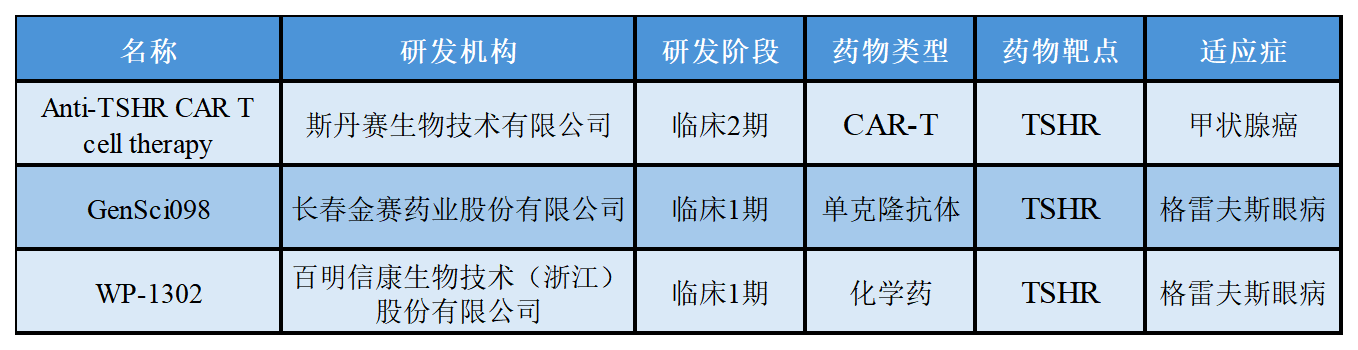
关于TSHR在研的部分药物进展如下表所示:
TSHR的细胞模型
为助力TSHR靶点药物研发,南京科佰开发了TSHR CRE-Luc HEK293、TSHR CHO细胞筛选模型,产品验证结果如下:
TSHR CRE-Luc HEK293CBP71485

Figure 3. Recombinant TSHR CRE-Luc HEK293 stably expressing TSHR.

Figure 4. Dose Response of Agonists in TSHR CRE-Luc HEK293(C31).
TSHR CHOCBP71474
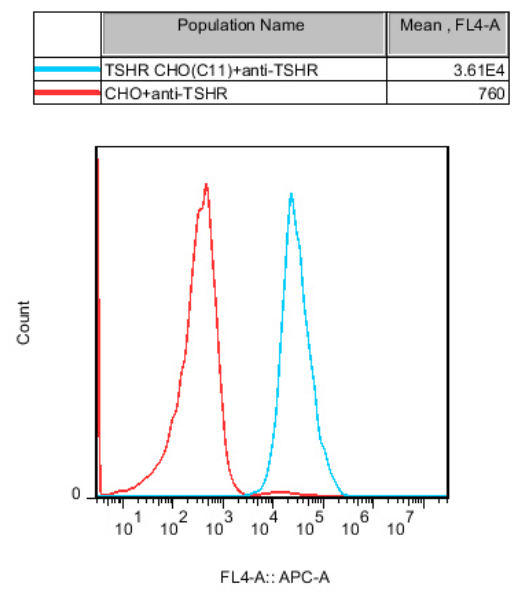
Figure 5. Recombinant TSHR CHO stably expressing TSHR.

Figure 6. HTRF cAMP Assay with TSHR CHO(C11).